金属有机框架材料吸附去除水中有机砷的研究进展
邓 圣,胡宇晗,杨 昱,韩 旭,夏 甫,肖 翰,鞠天宇,吴叔璇,徐祥健,姜永海
中国环境科学研究院,国家环境保护地下水污染模拟与控制重点实验室,北京 100012
众所周知,砷(Arsenic)是一种对所有生命体有毒有害的致癌物质,长期接触砷会给人体带来各种健康问题,如皮肤病变、心血管疾病、糖尿病和癌症,孕妇接触砷还将增加婴儿的死亡率[1-4]. 尽管在去除环境砷的研究领域中,科学家们已经开展了大量研究,但目前大多研究集中在无机砷的去除,而有机形式的砷却很少受到关注. 有机砷化合物作为饲料添加剂已广泛用于家禽养殖和畜牧业中以促进家禽的生长、提高饲料吸收率和控制肠道寄生虫[5-6]. 然而,有机砷化合物的大量使用对生态环境具有潜在危害,当水溶性有机砷〔如阿散酸(p-ASA)、洛克沙砷(ROX)等〕进入周围环境时,很容易通过生物降解或化学氧化转化为剧毒的无机砷(如亚砷酸盐和砷酸盐),导致土壤和地下水的污染[7-9],并随着食物链最终进入人体,危害人体健康[10-12]. 因此,环境中有机砷的高效处理是水处理领域亟需解决的难题,具有重要的环境意义[13].
虽然目前欧盟、美国和中国均禁止在动物饲料添加剂中使用有机砷,但是有机砷化合物在全世界大多数地方仍在使用,环境中有机砷污染的问题依旧存在. 研究估计超过数千吨的有机砷化合物通过养猪场和家禽养殖场的固体废物和废水排放到环境中,在土壤和水中检测出的有机砷浓度分别为0.2~1 000 μg/kg和0.5~5 000 μg/L,远超过世界卫生组织(WHO)对有机砷的标准限值. 目前,有机砷的去除方法主要有生物降解[14-15]、化学氧化法[16-17]和吸附法[18-19]等.相较于其他方法,吸附法因具有操作简单、去除率高、不产生高毒性中间产物等优点而受到研究者的广泛关注. 吸附法主要依靠于吸附剂的结构和特性,目前已经开发出多种针对有机砷的吸附剂,包括铁铝复合氧化物[20]、铁锰复合氧化物[21]、壳聚糖基共聚物[22]、多孔碳材料等. 然而这些材料对有机砷吸附动力学慢、吸附选择性有限、合成过程复杂,且材料化学和热稳定较差,限制其在有机砷去除中的应用. 金属有机框架(metal organic frameworks, MOFs)是一类由无机金属离子或金属簇和含氮、氧多齿有机配体通过强配位作用自主装形成的具有分子内孔隙的配位聚合材料,因其具有孔隙率高、比表面积大、孔道尺寸可调、易功能化改性和材料性能可定制等特点,已成为当前吸附材料领域的研究热点和前沿之一[23-24]. 目前已报道多种高化学稳定性和丰富功能化的MOFs材料用于水环境中无机砷或有机砷的高效去除. 无机砷〔如As(Ⅲ)和As(Ⅵ)〕主要通过静电和络合作用与MOFs材料发生吸附作用,而有机砷由于含有苯环、羟基、硝基和氨基等有机官能团,还能与MOFs材料通过氢键和π-π作用产生吸附作用,因此MOFs材料在有机砷的吸附去除中展现出更广阔的应用前景[25-27].
基于此,该文综述了国内外MOFs材料吸附去除有机砷的研究进展,归纳总结了不同类型MOFs(如单一MOFs、后修饰MOFs和MOFs基复合/衍生)材料的制备方法及其对有机砷的吸附去除性能,分析和讨论了MOFs材料对有机砷吸附的关键影响因素和吸附机理,并探讨了目前MOFs的技术缺陷,以及限制工程应用的关键因素和解决措施,为深入开展MOFs材料对水体中有机砷的去除研究提供参考.
1.1 单一MOFs材料
Jun等[28]首次报道了MOFs材料去除水体中有机砷化合物的研究,其采用微波辅助水热方法制备了3种不同中心离子(Fe、Cr和Al)的MIL-100材料,且发现3种材料对p-ASA和ROX均展现出更高的吸附效率. 另外,与活性炭、Y型沸石和针铁矿等常规吸附材料相比,MIL-100-Fe的吸附速率为活性炭吸附速率的4倍. 表征结果显示,尽管3种MOFs材料具有相似的结构组成和孔隙率,但MIL-100-Fe对p-ASA和ROX的吸附性能最佳,最大吸附量分别达到366和387 mg/g. DFT理论计算证实,这是因为水分子更容易从MIL-100-Fe中解吸,从而在MOF中产生更多配位不饱和金属位点(CUS)或开放金属位点(OMS),作为有机砷吸附位点. 除中心离子影响外,MOFs结构中的孔径结构同样影响有机砷的吸附效率. 大多数MOFs均为微孔结构(孔径小于2 nm),较小孔径阻碍了污染物扩散至MOFs结构内的吸附位点并与之发生作用,从而限制其吸附速率和吸附量.在MOFs材料中引入介孔,虽然降低了MOFs材料的比表面积,但较大的孔径和结构层次有利于污染物的传输扩散和吸附结合.p-ASA分子的大小(0.66 nm)与传统ZIF-8孔径尺寸(约为1.0 nm)较为接近,导致p-ASA在ZIF-8中的吸附速率不高,准二级动力学模型的吸附速率常数仅为2.2×10−3g/(mg·h). 为提升ZIF-8对p-ASA的吸附效率,Jung等[29]采用阳离子表面活性剂CTAB和L-组氨酸作为共模版,室温下制备了介孔修饰的ZIF-8,修饰后ZIF-8的孔径大小由1.0 nm提升至20~50 nm. 动力学吸附试验证明,相比于未修饰ZIF-8,介孔的引入有效提升ZIF-8对p-ASA的吸附速率,吸附速率是未修饰ZIF-8的4.4倍. 对比介孔修饰ZIF-8与未修饰ZIF-8、MIL-101-Cr、MIL-53-Cr、活性炭和Y型沸石等材料的吸附性能发现,尽管介孔ZIF-8的比表面积和总孔容积分别为1 134 m2/g和1.3 cm3/g,远小于MIL-101-Cr的3 574 m2/g和1.9 cm3/g,但对p-ASA的最大吸附量可达到791.1 mg/g,吸附量提升是由于ZIF-8孔径的增大,从而增加了其吸附位点的数量.
为探究MOFs材料对水环境中不同形态有机砷吸附效果的差异,Li等[30]采用溶剂热法,以FeCl3·6H2O和对苯二甲酸(BDC)为原料制备MIL-101-Fe,并研究其对水体中砷酸盐As(Ⅴ)、ROX、p-ASA和砷酸二甲酯(DMA)的吸附性能. MIL-101-Fe在ROX、p-ASA、DMA、As(Ⅴ)的吸附中均展现了良好的吸附性能,最大吸附量分别达到507.9、379.7、158.9和233.0 mg/g.动力学吸附结果表明,MIL-101-Fe对不同形态的砷均具有较高的吸附速率,4.0 h即可达到吸附平衡,这主要是由于其具有较大的孔隙率,污染物可快速扩散至其活性位点并发生相互作用. 不同形态砷的吸附速率依次为As(Ⅴ) > ROX >p-ASA> DMA,As(Ⅴ)、ROX和p-ASA的吸附速率受边界层扩散和颗粒内扩散控制,而DMA的吸附速率只受颗粒内扩散控制. 准二级动力学模型对吸附结果拟合较好,表明整个吸附过程中化学吸附占据主导. 相比较于其他MOFs材料,锆基MOFs材料在较宽pH范围的水溶液中具有很好的稳定性,是一种具有广阔应用前景的吸附材料.Lin等[31]考察了7种锆基MOFs材料(包括DUT-67、UiO-66、UiO-67、MOFs-808、MOFs-808F、NU-1000和NU-1000B)对有机砷的吸附性能,发现MOFs-808、MOFs-808F对p-ASA和ROX的吸附性能远高于其他几种MOFs及常见吸附材料,最大吸附量分别达到621.1、709.2 mg/g和649.4、641.0 mg/g. 而对于低浓度的p-ASA,MOFs-808F同样具有良好的吸附效果,去除效果几乎不受水体中其他干扰离子(Cl−、OAc−、SO42−)的影响,具有很高的选择性.
1.2 功能修饰MOFs材料
为了提高MOFs材料对有机砷的吸附效果和吸附速率,通过预先功能修饰或合成后修饰的方法制备改性MOFs材料也受到广泛的关注. 预先功能修饰是预先将有机配体修饰各种官能团,再与金属离子组装制备获得MOFs材料. 后修饰法是在MOFs材料合成后,通过对框架中的空金属位点进行配位修饰或者对有机配体进行原位修饰,引入一些官能团或功能性客体,从而在不改变原有结构的情况下,实现MOFs材料的功能化,满足设计需求[32-34].
由于有机砷结构复杂,通常含有氨基、羟基等可作为氢键位点的取代基,氢键作用是吸附去除有机砷的重要作用力之一. Sarker等[35]分别采用乙醇胺(ETA)和三乙醇胺(TEA)修饰MIL-101-Cr,成功制备了单羟基修饰的MIL-101-Cr(OH)和三羟基修饰的MIL-101-Cr(OH)3. BET表征结果表明,功能化过程中引入大量官能团导致MIL-101-Cr孔隙度有所下降.吸附试验结果表明,苯胂酸(PAA)和p-ASA的吸附量随材料中的羟基数量增加而升高. MIL-101-Cr(OH)3对PAA和p-ASA的最大吸附量分别为139和238 mg/g,分别为未修饰MIL-101-Cr吸附量的2.6和3.0倍,远优于活性炭的吸附效果. 与羟基类似,氨基同样是氢键受体,在MOFs中引入氨基不仅可增加活性位点,还能增强其他作用力强度. Lv等[36]采用溶剂热法,以2-氨基对苯二甲酸(H2ATA)为有机配体合成了六边形棒状NH2-MIL-68-In,FTIR和XPS分析结果均表明,引入的氨基基团增强了MIL-68-In与有机砷的氢键作用,从而提升了对有机砷的吸附性能、亲和力和吸附速率. NH2-MIL-68-In对p-ASA的吸附量及亲和力分别为502.5 mg/g和0.051 4 L/mg,高于MIL-68-In的446.4 mg/g和0.036 8 L/mg,吸附速率可以达到MIL-68-In的1.65倍.
MOFs材料中心金属离子簇与有机配体通常以饱和配位键连接,因此与有机砷通过金属配位作用的活性位点数量相对有限,在MOFs中制造缺陷形成不饱和金属配位点位,可为有机砷的吸附提供更多配位作用点位,增强配位吸附作用并提高吸附性能. Li等[37]选择结构稳定、缺陷易调控的锆基MOFs(UiO-66)作为研究对象,通过改变合成过程中调节剂苯甲酸的用量,调控UiO-66中金属核心簇缺陷的程度,制备得到4种缺陷数量可控的UiO-66高效吸附材料. 控制苯甲酸的投加量为0~20 mmol,在UiO-66中可相应地生成4.9~5.6个缺陷. 表征结果证明,缺陷修饰的UiO-66能有效提高其孔隙率〔见图1(a)〕,同时在MOFs结构中生成更高比例的高活性Zr-OH活性位点. 吸附试验证明,更高的孔隙率和更多的Zr-OH活性位点数量在ROX吸附中发挥重要作用,二者能有效增强修饰后UiO-66对ROX的吸附量和吸附速率.UiO-66-20对ROX的最大吸附量和吸附速率分别达到730 mg/g和5.26×10−3min−1,是未修饰UiO-66的3.7和21倍. 传统MOFs材料对有机砷的高吸附量大多基于较高的初始浓度,为提高低浓度有机砷的吸附效果,Xu等[38]采用溶剂热法,将1,4-苯二甲酸和ZrCl4溶解于DMF中,在220 ℃下加热16 h制备得到初始UiO-66,用盐酸洗涤UiO-66后,得到含有缺陷的UiO-66-D,并且以2-氨基苯二甲酸代替1,4-苯二甲酸通过相同的方法制得同时带有缺陷和氨基修饰的UiO-66-D-NH2. 表征结果表明,缺陷的产生和氨基的引入,并未改变其规则的八面体结构,结晶度和形态仍保持稳定〔见图1(b)〕. 吸附试验结果表明,UiO-66-D-NH2对有机砷的去除率随着污染物初始浓度的降低有逐渐增大的趋势〔见图1(c)〕. 在低初始浓度(1 mg/L)时,UiO-66-D-NH2对p-ASA和ROX的去除率分别为99.1%和99.2%,高于UiO-66-D(分别为98.0%、97.5%)和UiO-66(分别为93.9%、94.5%),吸附亲和力分别是原始UiO-66和UiO-66-D的3.8和3.0倍. 吸附去除效果几乎不受水体中其他干扰组分的影响,表现出优异的稳定性. Tian等[39]采用溶剂热法将不同数量的氨基引入具有缺陷的UiO-67的BPDC配体中,制备了两种缺陷和氨基共同修饰的UiO-67吸附剂. 表征结果表明,UiO-67、UiO-67-NH2(1)和UiO-67-NH2(2)中的缺陷数分别为4、3.2和3.2. 单位比表面积3种吸附剂的吸附量依次为UiO-67-NH2(2)>UiO-67>UiO-67-NH2(1),且UiO-67-NH2(2)对p-ASA的吸附亲和力是原始UiO-67的2倍. 在模拟天然废水条件下,添加0.15 g/L的UiO-67-NH2(2),可将水体中p-ASA的浓度从5 mg/L降至28.1 μg/L.
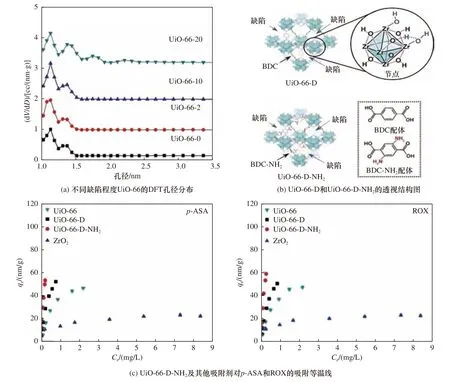
图 1 不同缺陷程度UiO-66的DFT孔径分布以及UiO-66-D、UiO-66-D-NH2的透视结构及其对有机砷的吸附等温线[37-38]Fig.1 DFT pore size distribution of UiO-66 with different defect levels and the perspective structure of UiO-66-D and UiO-66-D-NH2 and their adsorption isotherms of organic arsenics[37-38]
1.3 MOFs基复合/衍生材料
常规的MOFs应用水处理中存在易团聚、随水流流动流失大和回收困难等问题,将MOFs与其他材料复合可有效解决上述问题,如将MOFs与石墨烯复合可以增强MOFs在水溶液中的稳定性、导电性以及催化活性等性能. Pang等[40]将FeCl3·6H2O与富马酸混合搅拌24 h后制得水稳定性好的MIL-88A(Fe),分别采用合成后固定和原位生长2种方法,与棉纤维复合制备2种材料MC-1和MC-2. 相比较于合成后固定的方法,原位生长方法在棉纤维表面的分布更加密集〔见图2(a)〕. MIL-88A(Fe)对不同浓度的有机砷均展现了良好的吸附性能〔见图2(b)〕. 尽管复合后MC-1和MC-2的吸附速率要低于原始MIL-88A(Fe),但铁离子的泄露量明显降低,复合吸附材料的稳定性和重复使用性明显增强. 固定床吸附试验结果证明,MC-1或MC-2均可实现对有机砷污染物连续性去除. Zhu等[41]以MOFs Cu(Ⅰ)-tpp为原料,采用液相外延法制备得到ZIF-8紧密包裹的Cu(Ⅰ)-tpp@ZIF-8复合材料〔见图2(c)〕,对p-ASA具有优异的吸附性能和荧光检测性能. Cu(Ⅰ)-tpp@ZIF-8对p-ASA的吸附量可达到303.0 mg/g,检出限可达到0.4 μg/L. 由于MOFs材料独特的有机-无机框架结构,且结构和性能易于调节,使得其衍生复合材料特别是衍生碳复合材料在吸附去除污染物中受到广泛关注. Yu等[42]采用溶剂热法,在DMF溶液中加入Co(NO3)2·6H2O、FeCl3·6H2O和对苯二甲酸,搅拌后110 ℃加热24 h后合成Co-mil-101(Fe),将Co-mil-101(Fe)在800 ℃高温锻造4 h后制备了一种双金属复合催化剂Co-Fe@C,可高效活化过二硫酸盐(PDS)降解吸附p-ASA. 对比了Co-Fe@C与其他2种 催化剂Fe@C和Co@C对PDS的活化和去除效果,发现在pH=5、p-ASA初始浓度为20 mg/L时,0.2 g/L的Co-Fe@C与1.0 g/L的PDS混合5 min后,p-ASA即可完全降解去除,并且降解中产生的无机砷可被Co-Fe@C有效吸附,去除率达到93.40%,一步实现p-ASA的降解-吸附联合去除.
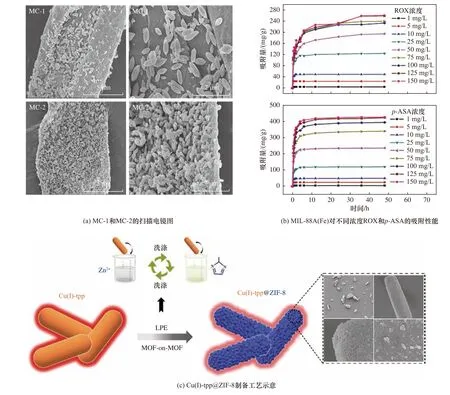
图 2 MIL-88A(Fe)与棉纤维的复合物表征及MIL-88A(Fe)对有机砷的吸附性能和Cu(Ⅰ)-tpp@ZIF-8制备工艺示意[40-41]Fig.2 Characterization of MIL-88A(Fe) decorated on cotton fibers and adsorption performance of MIL-88A(Fe) for organic arsenics and Schematic of the Cu(Ⅰ)-tpp@ZIF-8 fabrication process[40-41]
由于天然水体组成成分复杂,不同的成分可能会对水体中有机砷的存在形态、迁移转化和MOFs结构产生影响,并进一步影响MOFs对有机砷的吸附去除效果. 因此,有必要对水体中不同环境因子在吸附过程中所起到的效果进行探讨. 目前文献中探讨的影响MOFs吸附有机砷的主要水化学因素包含pH、共存离子及天然有机质.
2.1 pH
水环境中pH是影响MOFs对水体中有机砷吸附去除效果的重要因素之一. pH影响有机砷的存在形态和MOFs的稳定性,在pH < 1.9或 pH> 4.1时,p-ASA以阴离子形式存在,而当1.9 < pH<4.1时,p-ASA则表现为中性分子[36]. 同时,由于MOFs中心离子和有机配体之间配位键的可逆性,MOFs在水体中的稳定性较差,pH过低或过高时均会影响其稳定性[43]. 伴随着pH的改变,有机砷存在形态和表面电荷性质产生了变化,通过静电相互作用影响MOFs对有机砷的吸附效果. Lin等[31]研究发现,随着pH的增加,MOF-808对p-ASA的吸附呈现出先增后减的趋势,在pH=4时达到最高吸附量,表明过低或过高的pH均不利于对有机砷的吸附. Sarker等[35]所设计的UiO-66-D-NH2对p-ASA和PAA的吸附也呈现了相同的效果,吸附量随着pH升高呈现出先增后减的趋势,并在pH=4左右时达到最高.
不同pH下,MOFs对有机砷的吸附机制有所不同. 如Zhu等[41]研究了设计合成的Cu(Ⅰ)-tpp@ZIF-8对p-ASA的吸附机理,发现在酸性条件下,吸附主要以静电相互作用为主,而在其他pH条件下,则是以配位作用、氢键和π-π作用的协同作用为主;
Xu等[38]研究发现,UiO-66-D-NH2对p-ASA和ROX的吸附呈现出先增后减的趋势,随着pH的升高,二者之间的静电相互作用转化为静电斥力,吸附机制也随之改变.
2.2 共存离子
水体中除了目标污染物以外,还存在各种共存离子. 在吸附过程中,这些共存离子可能会与有机砷产生竞争,影响吸附效果. 不同共存离子对吸附的影响程度存在差异. Lin等[31]研究表明,在MOF-808对p-ASA的吸附过程中,Cl−的影响较小,而SO42−或OAc−则会使吸附效果显著降低. 当水体中SO42−达到p-ASA的5倍或20倍时,MOF-808对p-ASA的 吸 附 量 降至70%或54%左右. OAc−也展现出类似的抑制效果.此外,共存离子还可以通过改变水体中的pH从而影响吸附效果. Li等[30]研究表明,CO32−和SiO32−的存在对ROX和p-ASA的吸附有轻微的抑制作用,却对DMA的吸附有明显的增强作用. 该研究认为,可能是由于CO32−和SiO32−的水解,导致水体环境中的pH发生改变,进而影响MOFs对有机砷的吸附性能. 同时,共存离子的影响程度也与MOFs材料对有机砷的吸附机理有关. Li等[30]研究表明,由于MIL-101(Fe)对有机砷的主要吸附机理是Fe-O-As配位作用,吸附所形成的内球配合物使得吸附过程几乎不受电解质离子的影响. 因此,Cl−、NO3−、SO42−等水体中常见的阴离子对MIL-101-Fe的吸附性能影响较小,但具有与砷相似原子结构和化学性质的磷酸根(PO43−),则对有机砷的吸附产生了显著的影响. 由于二者吸附机理相似,在吸附过程中PO43−与有机砷产生竞争作用,降低吸附效果[44]. 吸附试验结果表明,在PO43−存在的情况下,MIL-101-Fe对ROX和p-ASA的吸附量分别降至初始吸附量的60%和50%左右.
2.3 天然有机质
溶解性有机物(DOM)是天然水体中普遍存在的污染物之一,对有机砷的吸附去除具有较大影响. 由于DOM中存在羧基、羟基和亚硫酸基等多种官能团,可与有机砷或MOFs中的芳香族基团发生静电、π-π作用等相互作用[20-45],在吸附过程中与有机砷产生竞争作用,影响吸附效果[46]. Li等[30]研究MIL-101-Fe对水体中不同砷化物的吸附性能时发现,在吸附过程中,溶解性有机物富里酸(FA)与ROX和p-ASA存在吸附竞争关系,导致MIL-101-Fe对二者的吸附量有所下降,而对不具备芳香基团结构的DMA,则几乎不产生影响. Tian等[39]研究UiO-67-NH2(2)对p-ASA的吸附效果时发现,随着水环境中DOM浓度的增加,UiO-67-NH2(2)对p-ASA的去除率略有下降,表明DOM与有机砷之间存在吸附竞争关系. Xu等[38]通过设计同时带有缺陷和氨基修饰的UiO-66-D-NH2,提高对水体中有机砷的吸附作用力,减少吸附过程中所受到吸附环境的影响. 如图3所示,随着水体中DOM浓度的升高,UiO-66-D-NH2对水体中有机砷的去除效果略有下降. 但是在低浓度条件下,DOM浓度对p-ASA和ROX的去除影响较小.
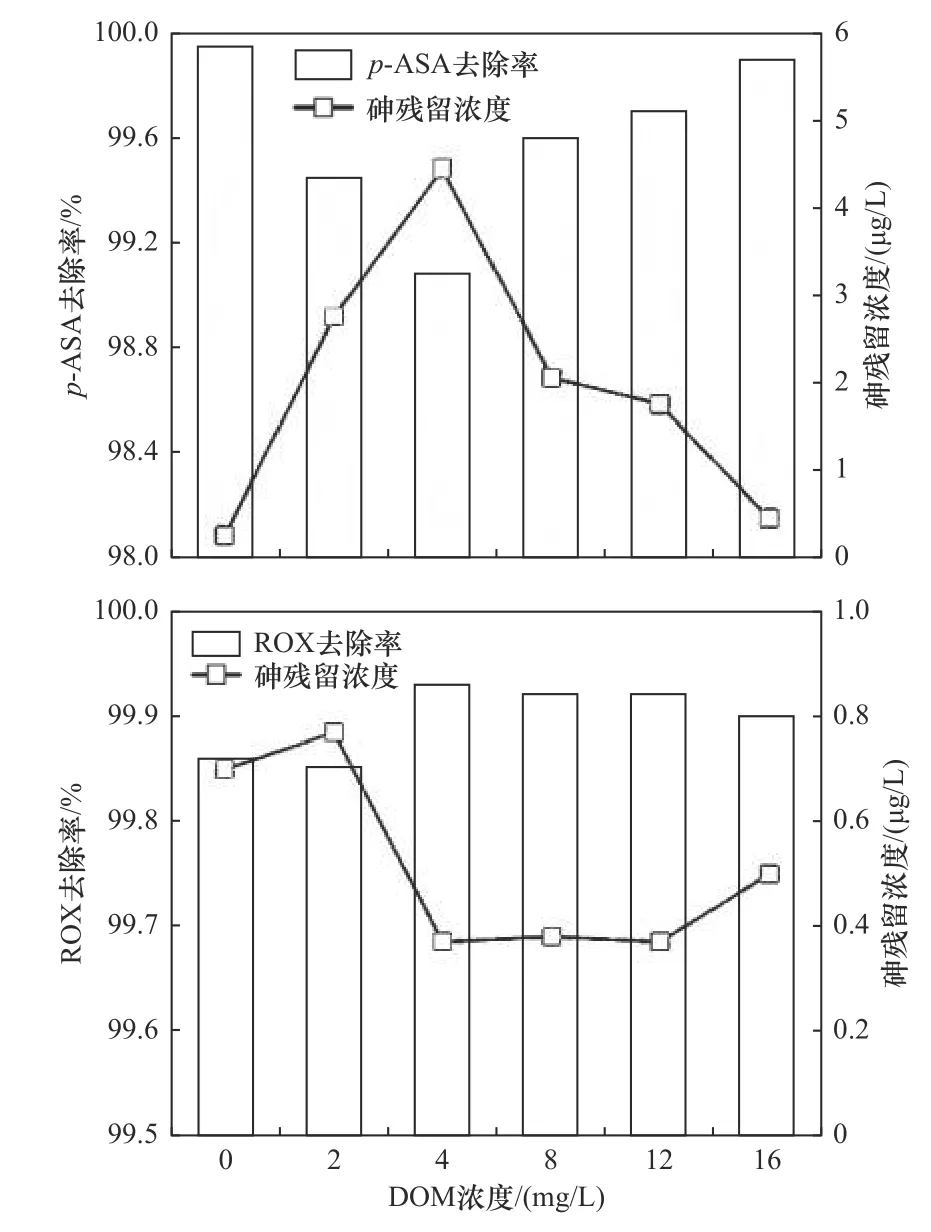
图 3 DOM浓度对UiO-66-D-NH2吸附ROX和p-ASA的影响[38]Fig.3 ROX and p-ASA adsorption performance by UiO-66-D-NH2 in the presence of DOM[38]
由于MOFs中存在的开放金属位点和多样的有机配体,在对有机砷的吸附过程中往往存在多种吸附机理并存的现象. 根据前人的报道,MOFs对有机砷的吸附机理主要包括静电作用、π-π作用、氢键作用、配位络合作用和多种机理协同作用[28-31,35,37,47].
3.1 静电作用
静电作用是由于吸附剂和被吸附离子之间带有相反电荷而产生的一种相互吸引作用,是水体中吸附去除污染物的一种常见吸附机制. 随着水环境中pH的改变,有机污染物往往会产生电离现象,与MOFs材料上的表面电荷产生吸引或排斥作用,从而影响MOFs对有机污染物的吸附效果[48]. Jung等[29]在研究介孔ZIF-8对p-ASA的吸附机理时发现,由于吸附的主要作用力是静电作用,介孔ZIF-8在不同pH条件下呈现出不同的吸附强度. 在pH为4.0~9.5范围内,带正电的ZIF-8对在此pH范围内均以阴离子形态(主要为H2NPhAsO32−)存在的p-ASA具有较强的吸附作用力. 而当pH<4.0或pH>9.5时,p-ASA主要以分子形态H2NPhAsO3H2存在或ZIF-8表面呈负电性,因此对p-ASA的吸附作用力均较弱.
3.2 π-π 作用
π-π作用是一种发生在芳香环之间的弱相互作用,在有机砷的吸附去除中常常发生于MOFs的有机配体与有机砷的苯环之间,以提高MOFs对有机砷的吸附效果. Li等[30]在研究MIL-101-Fe对水体中不同形态有机砷的吸附效果时,发现MIL-101-Fe中的1,4-苯二羧酸(BDC)配体与ROX和p-ASA中的芳香单元产生了π-π作用,增强了MIL-101-Fe对ROX和p-ASA的吸附效果.
3.3 氢键作用
氢键是存在于电负性较高原子的孤对电子与O−H等强极性键中氢原子之间的相互作用,是自然界中最常见的反应之一. 由于有机砷中常常含有氨基、羟基等可作为氢键位点的取代基,MOFs材料可以通过与具有合适官能团的配体直接合成或者合成后修饰,引入羟基、氨基等氢键取代位点,提高对有机砷的吸附作用和去除效果[47]. Sarker等[35]利用氨基醇对MIL-101进行羟基官能化,并合成了MIL-101(OH)3,其吸附机理如图4所示. 氨基的引入促进了以MIL-101(OH)3为供体,PAA和p-ASA为受体的氢键生成,使MIL-101(OH)3对有机砷的最大吸附量提高到原始MOFs材料的3.0倍.
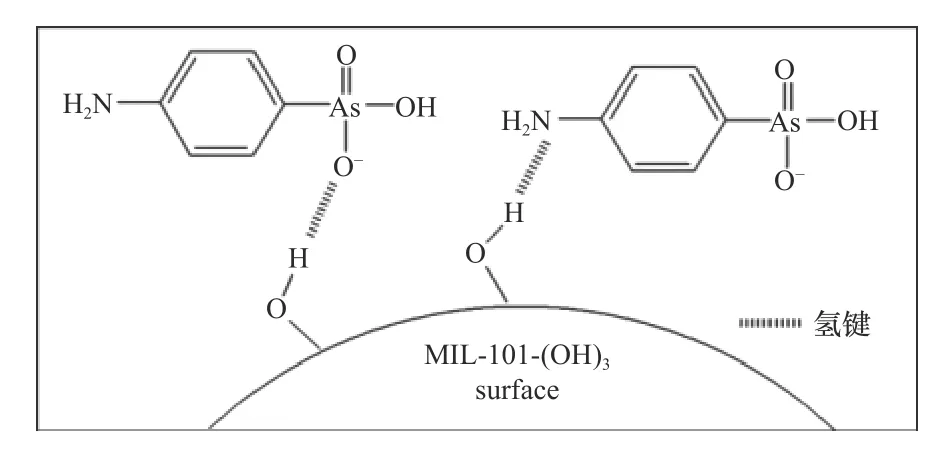
图 4 羟基功能化MOFs对有机砷的吸附机理[35]Fig.4 Adsorption mechanism of organic arsenics over hydroxyl functionalized MOFs[35]
3.4 配位络合作用
配位作用是通过配位双方一方提供空轨道,一方提供孤对电子形成配位键产生的结合作用,是无机砷在铁基材料上吸附的重要机制. 由于有机砷中含有与无机砷相似的结构,因此也是有机砷在MOFs材料中常见的吸附作用之一. Jun等[28]研究发现,MIL-100-Fe中CUS或OMS的基团易与有机砷生成As−O−Fe配位键,从而实现对有机砷的吸附. 而Li等[30]研究发现,MIL-101-Fe中的Fe离子与砷形成Fe−O−As配位键的过程中,砷分子中所含羟基的数量决定了其所能提供的配位位点的数量. 为了进一步加强MOFs材料与有机砷的配位作用,Li等[37]通过改变合成UiO-66中金属核心簇缺陷的程度,生成更高比例的高活性Zr-OH活性位点,与ROX形成更多As-O-Zr配位,提高吸附效果. 配位作用属于较强的作用力,在提高吸附效果的同时,也导致材料的重复利用率降低. Lin等[31]研究发现,对p-ASA的吸附以配位作用为主导的MOF-808为主,虽然其最大吸附量略高于以氢键、π-π作用和静电作用协同作用的MOF-808F,但在吸附特异性和可重复使用性上远逊于后者.
3.5 协同吸附作用
在MOFs材料对有机砷吸附去除的过程中,往往存在多种吸附机理协同作用. 为了提高去除效果,多采用对MOFs材料后修饰功能化引入相关官能团,引入或提升一种或多种吸附作用力,获得更佳的吸附性能. 另外,不同的作用机理有时也会产生相互影响.Xu等[38]通过将氨基引入存在缺陷的UiO-66-D,获得了对低浓度有机砷具有3倍亲和力的UiO-66-D-NH2.引入的氨基基团不仅促进氢键的生成,而且缩短了As-O-Zr配位距离,进一步增强配位作用. Tian等[39]通过将不同数量的氨基引入具有缺陷的UiO-67,也获得了相同的效果. 氨基的引入不仅为氢键作用提供了更多的位点,一方面通过缩短As与Zr原子的距离,形成更强的内球配合物;
另一方面也促进了π-π作用. 通过调控多种作用力产生协同作用,可以加强MOFs对有机砷的吸附作用力,达到强化吸附效果的目的. Zhu等[41]设计合成的Cu(Ⅰ)-tpp@ZIF-8首先与p-ASA发生氢键作用,随后二者之间的配位作用和π-π作用进一步加强吸附作用力;
同时,二者表面电荷所产生的静电引力与斥力也会影响吸附效果,其吸附机理如图5所示. Cu(Ⅰ)-tpp@ZIF-8复合材料对p-ASA的吸附是配位、氢键、静电和π-π作用协同作用的结果. 近年来不同类型的MOFs对有机砷的吸附机理和吸附性能如表1所示.
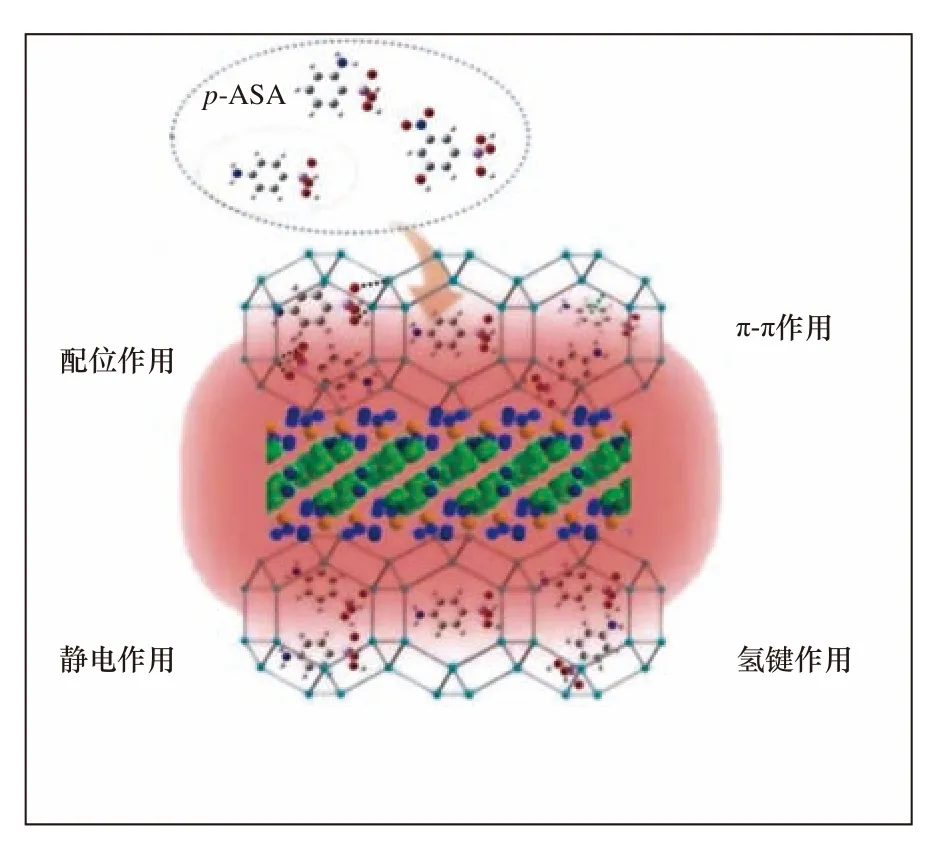
图 5 Cu(Ⅰ)-tpp@ZIF-8对p-ASA的吸附机理[41]Fig.5 Adsorption mechanism of p-ASA on Cu(Ⅰ)-tpp@ZIF-8[41]
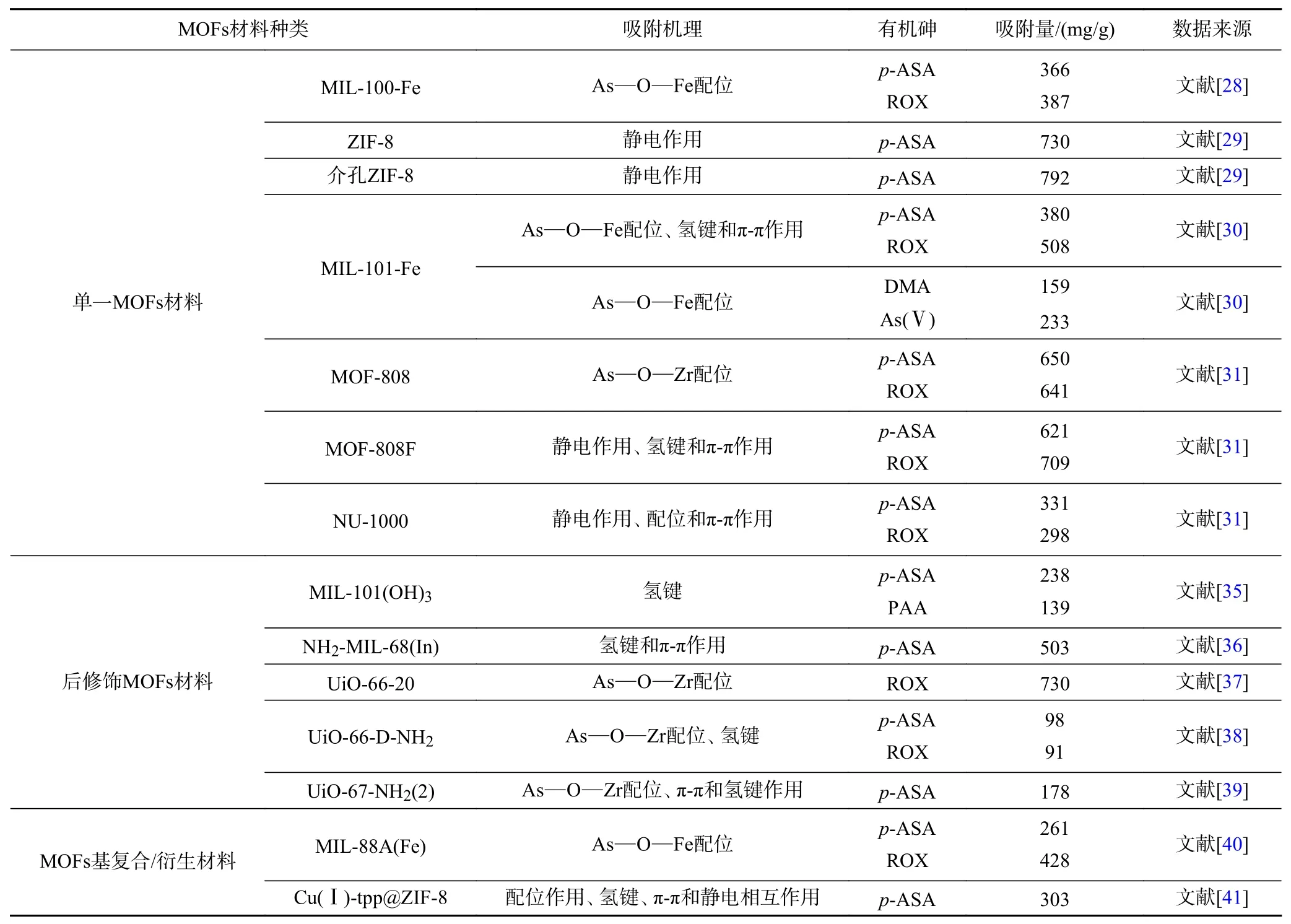
表 1 MOFs材料对有机砷的吸附性能比较Table 1 Comparison of adsorption properties of some MOFs for organic arsenics
从经济性和环境可持续性考虑,MOFs材料的再生性和稳定性是评价其吸附去除有机砷的两个关键要素,具有重要意义. 如表2所示,多种再生剂可用于洗脱吸附有机砷后的MOFs以达到再生目的,但不同溶剂对MOFs展现出不同程度的再生效果. 由于不稳定的MOFs结构影响材料的吸附量,因此合适的再生剂不仅能有效洗脱吸附于MOFs中的有机砷,同时还能维持MOFs的框架结构,保证循环使用中保留稳定的吸附性能.
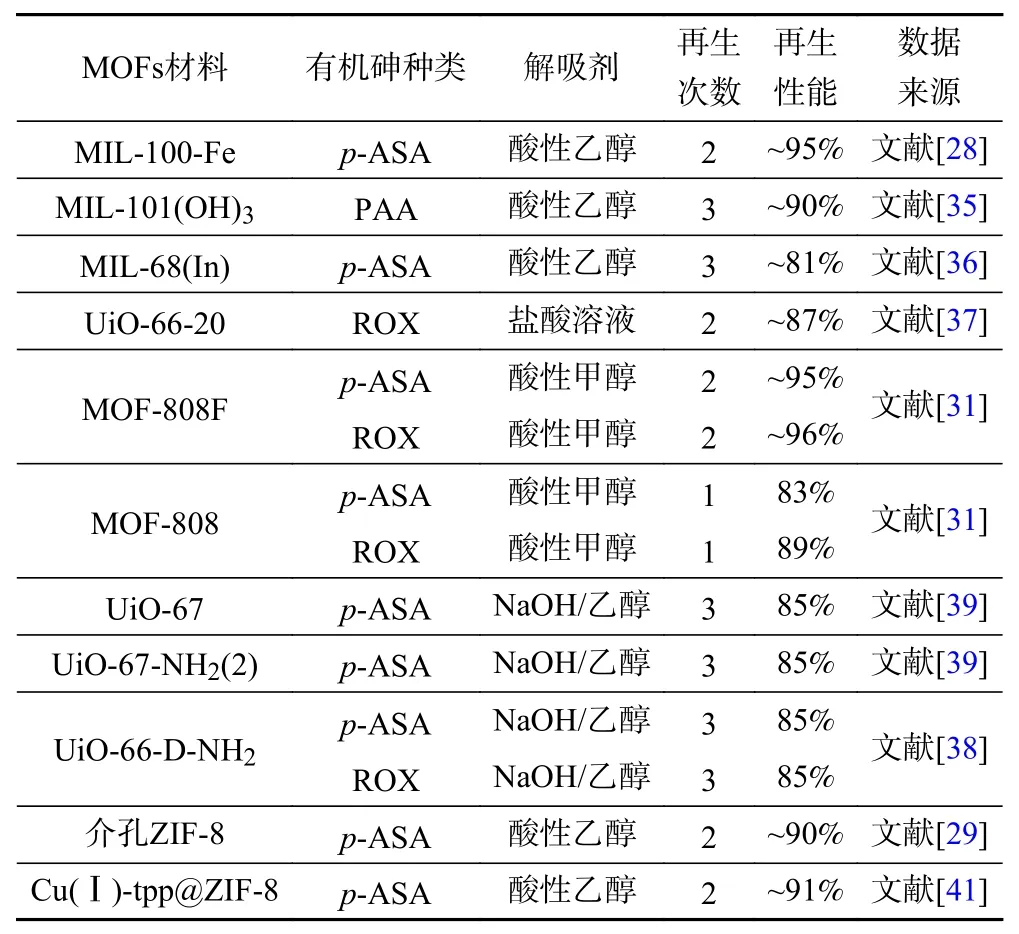
表 2 MOFs材料对有机砷的吸附循环再生性能Table 2 Adsorption and recycling properties of MOFs materials for organic arsenics
4.1 MIL系列MOFs
Jun等[28]研究了不同溶剂对MIL-100-Fe的再生性能影响. 典型的溶剂如乙醇、丙酮、甲醇和水对MIL-100-Fe的洗脱效果均较差,但在乙醇中加入少量的酸(0.1% HCl),可显著提高洗脱效果. 并且在3个循环后,MIL-100-Fe对p-ASA的吸附量无明显下降. 同时,FTIR光谱、XRD和氮气吸附均证实了再生后MIL-100-Fe的结构完整性. Sarker等[35]研究了酸性乙醇(含1% HCl)解吸MIL-101(OH)3的性能,红外表征结果发现,洗脱后位于1 440、1 313和1 097 cm−1处的PAA吸收峰均消失,证实酸性乙醇可快速高效洗脱吸附后的PAA. 3次循环后吸附剂的吸附性能未发生明显变化,吸附性能仅降低了10%. XRD分析表征证实,循环再生后MIL-101(OH)3仍保留完整的晶体结构,表明其具有良好的稳定性能. Lv等[36]合成的氨基修饰MIL-68(In)具有类似的再生效果. 采用酸性乙醇洗脱吸附p-ASA后的NH2-MIL-68(In),4次循环再生后去除率仅由约75%降至60%. 红外表征解吸后的吸附剂发现,解吸后p-ASA芳环中838 cm−1处的As−O和1 095 cm−1处的C−As键消失,证实已成功洗脱. XRD的表征结果与Sarker等[35]的研究结果一致,即循环再生后NH2-MIL-68(In)仍保留了完整的结构,MOFs材料具有良好的稳定性. 选择合适浓度的洗脱剂对MOFs材料的再生同样至关重要. Li等[30]研究了不同溶剂对MIL-101(Fe)的再生性能,分别选择2 mol/L NaCl、5 mmol/L NaOH、10 mmol/L HCl和NaOH作为洗脱剂,结果发现,2 mol/L NaCl仅有2%的洗脱效率,表明吸附并非通过简单的表面吸附或者外层络合作用. 5 mmol/L NaOH可有效再生MIL-101-Fe,再生后的吸附率为原始的80.21%,XRD结果证实,OH−与吸附质的离子交换作用是再生的主要机理. 然而当NaOH的浓度升至10 mmol/L后,尽管洗脱率可达100%,但高浓度NaOH溶解了MIL-101-Fe中的酸性有机联接桥配体,最终导致材料骨架结构分解.
4.2 锆系MOFs
研究表明,MOFs材料的水热稳定性受到金属与配体的各种性质的影响,其中二者的结合强度被认为是关键性因素. 根据软硬酸碱理论,Zr4+为硬酸,金属离子半径小,正电荷多且极化率小,易与N、O原子形成配位键. 因此,大多数锆基MOFs具有很强的水稳定性. Li等[37]将吸附饱和后的UiO-66-20浸泡在0.1 mol/L的HCl溶液中,通过酸的质子化作用达到解吸的目的,结果发现,ROX的解吸率在90%以上,循环3次后吸附量仅从347 mg/g降至302 mg/g,展现了良好的可重复利用性. Lin等[31]使用酸性甲醇(2 mol/L HCl)对MOF-808F和MOF-808进行索氏提取再生,洗脱剂中的甲醇可有效提取吸附的p-ASA,重复再生至少3次后,MOF-808F对p-ASA的吸附效率无明显降低. 值得一提的是,由于再生过程中MOF-808F中的部分配位甲酸阴离子会被水或羟基所取代,再生后的MOF-808F需在含有0.1 mol/L甲酸的DMF溶液中培养以补充框架中的有机配体. 与MOF-808F相比,再生后MOF-808对p-ASA和ROX的吸附率分别降至83%和89%,可重复利用性较差. Tian等[39]研究了NaOH/乙醇(0.5 mol/L)对UiO-67和UiO-67-NH2(2)的解吸性能,4次循环再生后,二者对p-ASA仍保持着原容量85%以上的吸附量. XRD分析表征证实,循环再生后UiO-67和UiO-67-NH2(2)的晶体结构均没有发生变化. 同时,FTIR分析结果证实,UiO-67-NH2(2)中的−NH2在重复吸附过程中保持稳定,解吸过程不会影响所引入氨基的稳定性. Xu等[38]使用NaOH/乙醇(0.5 mol/L)对UiO-66-D-NH2进行的解吸试验也具有相同的效果. 4次循环再生后,UiO-66-D-NH2对p-ASA和ROX的吸附量均不低于初始吸附量的85%. 同时,XRD和FTIR的表征结果与Tian等[39]的研究结果一致,晶体结构和官能团均未发生变化.
4.3 其他系列MOFs
Jung等[29]使用酸性乙醇(pH=4)洗涤介孔ZIF-8,XRD、氮气吸附和FTIR分析结果证实了介孔ZIF-8解吸之后并无p-ASA的残留并且结构完整. 重复洗脱再生3次后,吸附率仍可达到原始吸附率的90%左右. 在Zhu等[41]所设计Cu(Ⅰ)-tpp@ZIF-8对p-ASA的特异性检测和去除研究中,同样使用酸性乙醇进行解吸,重复运行3次后,吸附量只是略有降低,仍能达到原始吸附量的91%左右. PXRD谱图分析证实,p-ASA洗脱后Cu(Ⅰ)-tpp@ZIF-8的结构保持完整.
简单、高效去除水体中有机砷特别是低浓度有机砷具有重要意义,作为近年来新兴热点材料,MOFs由于其高孔隙率和大比表面积、易于修饰等特性,在水中有机砷污染处理中具有广阔的应用前景. 然而目前对于MOFs处理有机砷的研究仍处于初级阶段,在具体应用中还存在一些技术缺陷和限制其工程应用的关键因素,主要包括:①MOFs水稳定差. 水环境中MOF材料的有机配体易被水分子逐步取代,最终导致骨架的崩塌. 水稳定性仍然是阻碍大多数MOF材料实际应用的一大挑战. ②制备MOFs的金属或有机配体本身为对环境有毒害物质. MOFs在水体中降解后释放重金属或有毒有害的有机配体增加水中次生环境风险. ③应用形式单一. 目前大多数研究均直接采用MOFs材料吸附去除有机砷,实际应用中材料不易回收增加使用成本,且无法长效发挥材料使用性能. ④MOFs单次产率低、宏量制备困难,且再生实用性较差. 针对上述关键问题,未来应考虑从以下几个方面解决:
a) 在维持MOF原有孔特性和吸附活性位暴露的前提下,提升水敏感MOFs的稳定性. 在MOFs材料表面修饰疏水表面层或与壳聚糖等材料交联可有效提升MOFs材料的水稳定性.
b) 选择安全、稳定的基元材料制备MOFs,以降低其在实际水环境应用时受水中污染物、金属盐或离子影响而解离造成次生环境风险,提高MOFs的再生循环使用性能. 同时还需在复杂成分水体或连续流条件下考察MOFs材料中有机配体或金属的潜在泄露风险.
c) 应开发更简便的MOFs材料合成方法,如采用电化学方法或离子液体辅助的球磨方法实现MOFs低成本宏量化生产,以提供更适用于实际的应用材料.
d) 将MOFs材料与其他材料如磁性材料、膜材料等复合制备MOF基复合材料,可解决MOFs材料实际应用过程中易团聚且难以回收的问题,并延长其使用寿命.
e) 目前有机砷的吸附研究主要集中在少数种类的MOFs,需要探索更多种类的合适MOFs. 作为一种新兴热点材料,MOFs材料中配位环境、配位方式、金属及配体的多样性和可设计性等赋予其丰富多彩的构型. 未来应以“理论机制解析−材料结构调控−性能评估验证”为主线,层次递进开展高吸附性能MOFs材料研发.
猜你喜欢 氢键配体氨基 (H2O)n,(H2O)n- ,H(H2O)n+ (n=1~6) 电子结构的理论研究河北师范大学学报(自然科学版)(2022年5期)2022-09-204-酰基吡唑啉酮-5缩γ-氨基丁酸衍生物的合成及对白玉菇菌丝脱氢酶活性影响天津农学院学报(2022年2期)2022-08-05一个镉配合物[Cd(H2O)(L)(HBTC)]·H2O的合成,结构和荧光性能渤海大学学报(自然科学版)(2022年1期)2022-07-25高效阴离子交换-积分脉冲法检测氨基寡糖素农药中游离氨基葡萄糖农药学学报(2022年3期)2022-06-14利用氨基功能化电极材料除磷及动力学探究节能与环保(2022年3期)2022-04-263%甲氨基阿维菌素微乳剂注干剂配方研究安徽农学通报(2022年6期)2022-04-07盐酸四环素中可交换氢和氢键的核磁共振波谱研究波谱学杂志(2021年3期)2021-09-07一个氢键构筑的基于偶氮二羧酸和吡啶酰胺配体的超分子配合物渤海大学学报(自然科学版)(2020年3期)2020-02-02基于[2,2]对环芳烷骨架手性配体的设计、合成及其在不对称反应中的应用研究进展报告科技创新导报(2016年30期)2017-03-15氨基葡萄糖会导致血糖升高吗家庭用药(2016年8期)2016-05-14- 范文大全
- 说说大全
- 学习资料
- 语录
- 生肖
- 解梦
- 十二星座
-
主题党日活动交流发言8篇
主题党日活动交流发言8篇主题党日活动交流发言篇13月13日,东城区党史学习教育动员大会召开。市委
【活动总结】 日期:2022-12-23
-
家乡赋|最美的家乡赋
家乡赋 孙传志 今安康市,白河双丰镇,吾之家乡也。三环沃土,山水环抱。其北依山,山系五岭,山
【调研报告】 日期:2020-04-01
-
【人教版1-6年级数学上册知识点精编】1-6年级数学人教版教材
人教版二年级数学上册知识点汇总第一单元长度单位一、米和厘米1、测量物体的长度时,要用统一的标准去测量
【调研报告】 日期:2020-11-08
-
2022年2月份主题党日活动记录5篇
2022年2月份主题党日活动记录5篇2022年2月份主题党日活动记录篇1尊敬的党组织:在今年的开学初,本人积极参加教研室组织的教研活动,在学校教研员的指
【活动总结】 日期:2022-08-12
-
5,x党支部主题党日活动记录(范文推荐)
支部一词应该来自于天干地支,干部一词亦同。如“己丑”,天干部分为己,只代表天干己自己,不包括其它,而地支部分丑则包括“癸辛己”三个天干。所以干部是指起骨干作...
【活动总结】 日期:2023-01-04
-
2023年平安校园建设方案13篇
平安校园建设方案“平安校园”创建工作,我们幼儿园全体教职员工一直把它当作头等大事来抓。领导高度重视,以“平安校园”创建活动为抓手,建立和规范校园安全工作机制
【规章制度】 日期:2023-11-02
-
医院最佳主题党日活动11篇
医院最佳主题党日活动11篇医院最佳主题党日活动篇1 医院最佳主题党日活动篇2为隆重纪念中国共产党成立100周年,进一步巩固党的群众路线教育实践活动成果,切实
【活动总结】 日期:2022-10-29
-
南京大屠杀国家公祭日悼念文案句子11篇
南京大屠杀国家公祭日悼念文案精选句子1、惟有民魂是值得宝贵的,惟有他发扬起来,中国才有真进步。——鲁迅2、我爱我的祖国,爱我的人民,离开了它,离开了他们,我
【企划文案】 日期:2023-10-20
-
主题党日活动记录202210篇
主题党日活动记录202210篇主题党日活动记录2022篇12021年是中国共产党成立100周年,为广泛开展爱国主义宣传教育,铭记党的历史,讴歌党的光辉历程,
【活动总结】 日期:2022-08-02
-
医院收费人员工作违纪检讨书:干部检讨书
尊敬的院领导:事发于xx年xx月xx日晚,由于对新系统操作的不熟悉,致使年终医保结算工作拖沓不前,无法在正常的上班工作时间内完成。于是院领导安排我当晚加班结算x年尚...
【活动总结】 日期:2019-08-07
-
一年级新学期目标简短_一年级学生新学期打算
新学期到了,我是一年级下册的小学生了。 上课的时候,我要认真学习,不做小动作,认真听讲。我要认真学习,天天向上,努力学习,耳朵要听老师讲课,眼睛要瞪得大大的看老...
【简历资料】 日期:2019-10-26
-
[信访复查复核制度作用探讨]信访复查复核有用吗
作为我国特有的一项制度,信访制度的出现并长期存在不是偶然的,虽然一些法学专家认为信访制度具有“人治”
【职场指南】 日期:2020-02-16
-
[党员干部2019年主题教育个人问题检视清单及整改措施2篇] 党员干部
2019年主题教育问题检视清单及整改措施根据主题教育领导小组办公室《关于认真做好主题教育检视问题整改
【求职简历】 日期:2019-11-08
-
网络维护工作内容_(精华)国家开放大学电大专科《网络系统管理与维护》形考任务1答案
国家开放大学电大专科《网络系统管理与维护》形考任务1答案形考任务1理解上网行为管理软件的功能【实训目
【职场指南】 日期:2020-07-17
-
民族团结的素材资料13篇
民族团结的素材资料13篇民族团结的素材资料篇1研究进一步推进新疆社会稳定和长治久安工作。会议指出,要全面贯彻执行党的民族政策,把民族团结作为各族人民的生命线
【简历资料】 日期:2022-08-16
-
党委会与局长办公会的区别_局长办公会制度
为进一步加强xxx局工作的规范化、制度化建设,提高行政效能,规范议事程序,特制定本制度。一、会议形式1、局长办公会议由局长、副局长参加。由局长召集和主持。根据工作需要...
【求职简历】 日期:2019-07-30
-
红旗颂朗诵稿原文【《红旗颂》朗诵词】
《红旗颂》朗诵词 女:晴空万里,红旗飘扬, 六十载风云,我们昂首阔步。 男:六十个春秋,
【职场指南】 日期:2020-02-16
-
如何凝心聚力谋发展【坚定信心谋发展凝心聚力促跨越】
当前,清河正处于在苏北实现赶超跨越基础上全面腾飞的战略机遇期,处于在全市率先实现全面小康基础上率先实
【简历资料】 日期:2020-03-17
-
学生会组织部部长竞选稿5篇
学生会组织部部长竞选稿以“三制”为统领推进农村党的建设中共**市委组织部近年来,**市认真落实中央、省和徐州市委的部署,积极适应发展要求,从加强领导体制、运
【求职简历】 日期:2023-11-06
-
《铁拳砸碎“黑警伞”》警示教育片观后感
影片深刻剖析了广西北海市公安局海西派出所原所长张枭杰蜕变堕落的轨迹。观看警示教育片后,做为一名党员教
【简历资料】 日期:2020-08-17
-
X镇城市基层党建工作开展情况汇报
按照会议安排,现就我镇城市基层党建工作开展情况简要汇报如下:一、基本情况xx镇辖xx个城镇社区,共有
【节日庆典】 日期:2020-12-18
-
百年党史中的重大事件4篇
百年党史中的重大事件4篇百年党史中的重大事件篇1党史专家李颖所著的《文献中的百年党史》(学林出版
【其他范文】 日期:2022-12-19
-
2022年在党支部书记抓基层党建工作述职评议会上的讲话【完整版】
在党支部书记抓基层党建工作述职评议会上的讲话同志们:根据党委党建工作部署,今天召开2021年度党支部书记抓基层党建工作述职评议会。党委对标对表中央新的要求,进一步加强...
【其他范文】 日期:2022-11-07
-
【建设局局长就职演说】 建设局局长
Ztg154{display:none;}各位领导、同志们: x月xx日,市14届人大常委会第23次会议任命我为市建设委员会主任,接到任命书后,我想的很多。市委、市人大常委会、市政府将这么...
【节日庆典】 日期:2019-09-21
-
年党史学习教育民主生活会对照检查发言提纲(全文完整)
2021年民主生活会对照检查发言提纲根据市委办公室关于召开专题民主生活会的有关要求,会前经过深入学习研讨,广泛征求意见建议,诚恳谈心谈话,在此基础上,把自己摆进去、把...
【其他范文】 日期:2022-10-09
-
2020医务人员抗击疫情心得体会
敬爱的白衣天使:你们好!2020年春节如约而至,全国人民正沉浸在新年的喜悦中,忙采购、忙打扫、忙欢聚
【节日庆典】 日期:2020-09-02
-
2022年度【形容无聊句子说说】形容无聊爆笑说说
当前位置:>>>>2021-10-04说说可以为大家带来当日心情和好优美句子分享,是一个分享自己平台。下面就是小编整理形容无聊爆笑说说,一起来看一下吧。一、或许我有点无聊,常希望...
【其他范文】 日期:2022-10-27
-
基于GIS建模的配网变电设计及工程管理研究*
李清,杨骏涛,陶燕(1 国网上海市电力科学研究院,上海200540;2 国网上海金山供电公司,上海2
【其他范文】 日期:2023-01-19
-
2023在打造模范机关推进会上讲话(2023年)
同志们:打造模范机关是党中央、省委、市委和县委提出的一项重要政治任务,是推动新时代机关党建高质量发展的重要抓手,是服务改革发展稳定大局的现实需要。大家要从政治和全...
【其他范文】 日期:2024-02-06
-
人力资源论文范本5篇
人力资源论文范本5篇人力资源论文范本篇1小时候看《小马过河》这篇故事很有趣,而且有着深刻的哲理,对我们的学习和生活有很大的启发和帮助。故事说的是:小马准
【毕业论文】 日期:2022-09-02
-
军转座谈会交流发言4篇
军转座谈会交流发言4篇军转座谈会交流发言篇1大家好,我叫贺丽,2015届选调生,来自康定市委组织部,现在省委编办跟班学习。今天,非常荣幸向大家汇报我的学习收
【发言稿】 日期:2022-10-27
-
理论中心组学习总体国家安全观发言材料9篇
理论中心组学习总体国家安全观发言材料9篇理论中心组学习总体国家安全观发言材料篇1(八)深入学习贯彻中央以及省的重要会议和文件精神深入学习贯彻年度内中央以
【发言稿】 日期:2022-08-04
-
12岁生日小寿星发言4篇
12岁生日小寿星发言4篇12岁生日小寿星发言篇1各位来宾、各位朋友:大家好!今天,我们欢聚在这里,共同庆祝**十二周岁生日。首先,我代表**的父母以
【发言稿】 日期:2022-07-31
-
乡村治理交流发言材料6篇
乡村治理交流发言材料6篇乡村治理交流发言材料篇1为了进一步加大我镇农村环境综合治理力度,全面提升农村环境品质,对照农村环境综合治理“三整治一改造”的任务要求
【发言稿】 日期:2022-10-23
-
党内警告处分党员讨论发言3篇
党内警告处分党员讨论发言3篇党内警告处分党员讨论发言篇1大家好!作为新时期的一名大学生,认真学习、深刻领会、全面贯彻省党代会精神,是当前和今后一个时期重
【发言稿】 日期:2022-08-07
-
2023年今日新闻摘抄十条3篇
今日新闻摘抄十条大家一定记得七月初时的洪水,那可是轰动一时的大事呢!抗洪救灾的官兵跑在了前线,大家也在密切关注着动向。突如其来的洪水是很多人措手不及,瞬间就
【贺词】 日期:2023-10-14
-
廉政大会总结发言稿7篇
廉政大会总结发言稿7篇廉政大会总结发言稿篇1各位领导,同志们:根据会议安排,我就党风廉政建设工作做表态发言,不妥之处,请批评指正。一、提高认识,切实
【发言稿】 日期:2022-10-30
-
2023年批评与自我批评发言稿简短12篇
批评与自我批评发言稿简短根据市委、区委及局机关统一部署,开展多次党的群众路线教育实践活动。活动紧紧围绕保持党的先进性和纯洁性,遵照提出的“照镜子、正衣冠、洗
【发言稿】 日期:2024-01-02
-
纪委书记工作表态发言4篇
纪委书记工作表态发言4篇纪委书记工作表态发言篇1在镇党委政府正确领导下,在全村干部和群众的共同努力下,紧紧围绕建设社会主义新农村工作为重点,尽职尽责,与时俱
【发言稿】 日期:2022-09-30
-
我最敬佩的人开头_我敬佩的一个人作文20篇2020年
我敬佩的一个人作文20篇 我敬佩的一个人作文一): 我身边有很多值得我们敬佩的人,但我最敬佩的一
【发言稿】 日期:2020-11-10
-
2023年中国行政区划调整方案(设想优秀3篇
中国行政区划调整方案(设想优秀民政部第二次行政区划研讨会会议内容一、缩省的意义与原则1.意义1)利于减少中间层次中国行政区划层级之多为世界之最,既使管理成本
【周公解梦】 日期:2024-02-20
-
学习周永开先进事迹心得体会3篇
学习周永开先进事迹心得体会【一】通过学习周永开老先生先进事迹后,结合自己工作思考,感慨万千。同样作为
【格言】 日期:2021-04-10
-
XX老干局推进党建与业务深度融合发展工作情况调研报告:党建调研报告
XX老干局推进党建与业务深度融合 发展工作情况的调研报告 党建工作与业务工作融合发展始终是一个充满生
【成语大全】 日期:2020-08-28
-
中国共产党第三代中央领导集体的卓越贡献
中国共产党第三代中央领导集体的卓越贡献 --------------继往开来铸就辉煌 【摘要】改
【成语大全】 日期:2020-03-20
-
信息技术2.0能力点 [全国中小学教师信息技术应用能力提升工程试题题库及参考答案「精编」]
全国中小学教师信息技术应用能力提升工程试题题库及答案(复习资料)一、判断题题库(A为正确,B为错误)
【格言】 日期:2020-11-17
-
党建工作运行机制内容有哪些_构建基层党建工作运行机制探讨
党的基层组织是党在社会基层组织中的战斗堡垒,是党的全部工作和战斗力的基础。加强和改进县级以下各类党的
【经典阅读】 日期:2020-01-22
-
集合推理_七,推理与集合
七推理与集合1 期中考试数学成绩出来了,三个好朋友分别考了88分,92分,95分。他们分别考了多少分
【名人名言】 日期:2020-12-18
-
电大现代教育原理_最新国家开放大学电大《现代教育原理》形考任务2试题及答案
最新国家开放大学电大《现代教育原理》形考任务2试题及答案形考任务二一、多项选择题(共17道试题,共3
【成语大全】 日期:2020-07-20
-
基层党务工作基本内容_党建基本工作有哪些
党建基本工作有哪些(一) 基层党建工作包括哪些内容 选择了大学生村官这条路,你就与农村基层党
【名人名言】 日期:2020-08-06
-
【2020-2021学年高一英语外研版(2019)选择性必修第一册Unit3Faster,higher,strongerSectionⅠ导学讲义】
Unit3 Faster,higher,stronger背景导学MichaelJordan—Head
【歇后语】 日期:2021-04-19
-
关于三农工作重要论述心得体会3篇
关于三农工作重要论述心得体会3篇关于三农工作重要论述心得体会篇1习近平总书记指出:“建设现代化国家离不开农业农村现代化,要继续巩固脱贫攻坚成果,扎实推进乡村
【学习心得体会】 日期:2022-10-29
-
坚持和平发展道路,推动构建人类命运共同体心得体会10篇
坚持和平发展道路,推动构建人类命运共同体心得体会10篇坚持和平发展道路,推动构建人类命运共同体心得体会篇1本次青年大学习主题聚焦于构建人类命运共同体重要战略
【学习心得体会】 日期:2022-08-12
-
社区矫正人员学法心得体会汇报8篇
社区矫正人员学法心得体会汇报8篇社区矫正人员学法心得体会汇报篇1为扎实开展社区矫正工作,加强社区服刑人员监督管理,帮助其增强社会责任,8月17日,锡林浩特市
【学习心得体会】 日期:2022-10-27
-
【福生庄隧道坍塌处理方案】 福生庄隧道在哪里
(呼和浩特铁路局大包电气化改造工程指挥部,内蒙古呼和浩特010050)摘要:文章介绍了福生庄隧道
【学习心得体会】 日期:2020-03-05
-
五个一百工程阅读心得体会13篇
五个一百工程阅读心得体会13篇五个一百工程阅读心得体会篇1凡益之道,与时偕行。在全国网络安全和信
【学习心得体会】 日期:2022-12-07
-
双拥手抄报内容 [双拥标语300则]
双拥标语300则 1、开展双拥共建,构建和木垒。 2、坚持党对军队的绝对领导,走中国特色的精兵之
【培训心得体会】 日期:2021-10-27
-
城管系统警示教育心得体会9篇
城管系统警示教育心得体会9篇城管系统警示教育心得体会篇1各党支部要召开多种形式的庆七一座谈会,组织广大党员进行座谈,回顾党的光辉历程,畅谈党的丰功伟绩,
【学习心得体会】 日期:2022-10-09
-
参观新疆革命烈士纪念馆心得体会8篇
参观新疆革命烈士纪念馆心得体会8篇参观新疆革命烈士纪念馆心得体会篇1铮铮铁骨,万千英魂,诉不尽战
【学习心得体会】 日期:2022-12-08
-
党的方针政策心得体会7篇
党的方针政策心得体会7篇党的方针政策心得体会篇1xx年以来,本支部严格按照规定的时限和要求传达贯彻落实中央、上级党组织和学校党委有关文件和重要会议精神。制定
【学习心得体会】 日期:2022-08-03
-
2022年全国检察长会议心得7篇
2022年全国检察长会议心得7篇2022年全国检察长会议心得篇1眼睛是心灵上的窗户,我们通过眼睛才能看到世间万物,才能看到眼前这美好的一切。拥有一双明亮的眼
【学习心得体会】 日期:2022-10-31
-
 2024年主题教育民主生活会批评与自我批评意见(38条)(范文推荐)
2024年主题教育民主生活会批评与自我批评意见(38条)(范文推荐)
2023年主题教育民主生活会六个方面个人检视、相互批评意见:1 理论学习系统性不强。学习习近平新时代中国特色社会主义思想不深不透,泛泛而学的时候多,深学细照的时候少,特...
【邓小平理论】 日期:2024-03-19
-
 2024年交流发言:强化思想理论武装,增强奋进力量(完整)
2024年交流发言:强化思想理论武装,增强奋进力量(完整)
习近平总书记指出:“一个民族要走在时代前列,就一刻不能没有理论思维,一刻不能没有思想指引。”党的十八大以来,伴随着新时代中国特色社会主义思想在实践中形成发展的历程...
【三个代表】 日期:2024-03-19
-
 2024年度镇年度县乡人大代表述职评议活动总结
2024年度镇年度县乡人大代表述职评议活动总结
xx镇20xx年县乡人大代表述职评议活动总结为响应县级人大常委会关于开展县乡两级人大代表述职评议活动,进一步激发代表履职活力,加强代表与人民群众的联系,提高依法履职水平...
【马克思主义】 日期:2024-03-19
-
 “千万工程”经验学习体会(研讨材料)
“千万工程”经验学习体会(研讨材料)
“千万工程”是总书记在浙江工作时亲自谋划、亲自部署、亲自推动的一项重大决策,也是习近平新时代中国特色社会主义思想在之江大地的生动实践。20年来,“千万工程”先后经历...
【三个代表】 日期:2024-03-19
-
 2024年在市政协机关工作总结会议上讲话
2024年在市政协机关工作总结会议上讲话
同志们:刚才,XX同志对市政协机关20XX年工作进行了很好的总结,很精炼,很到位,可以感受到去年机关工作确实可圈可点。XX同志宣读了表彰决定,机关优秀人员代表、先进集体代...
【邓小平理论】 日期:2024-03-18
-
 在全区防汛防涝动员暨河长制工作推进会上讲话提纲【完整版】
在全区防汛防涝动员暨河长制工作推进会上讲话提纲【完整版】
区长,各位领导,同志们:汛期已经来临,我区城区防涝工作面临强大考验,形势不容乐观。年初,区城区防涝排渍指挥部已经召开专题调度会,修订完善应急预案,建立网格化管理机...
【马克思主义】 日期:2024-03-18
-
 2024年镇作风整治工作实施方案(完整文档)
2024年镇作风整治工作实施方案(完整文档)
XX镇作风整治工作实施方案为深入贯彻落实党的二十大精神及省市区委深化作风建设的最新要求,突出重点推进干部效能提升,坚持不懈推动作风整治工作纵深发展,根据《关于印发《2...
【毛泽东思想】 日期:2024-03-18
-
 2024市优化法治化营商环境规范涉企行政执法实施方案【优秀范文】
2024市优化法治化营商环境规范涉企行政执法实施方案【优秀范文】
xx市优化法治化营商环境规范涉企行政执法实施方案为持续优化法治化营商环境,激发市场主体活力和社会创造力,规范行政执法行为,创新行政执法方式,提升行政执法质效,着力解...
【毛泽东思想】 日期:2024-03-18
-
 2024年度关于开展新一轮思想状况摸底排查工作通知(完整)
2024年度关于开展新一轮思想状况摸底排查工作通知(完整)
关于开展新一轮思想状况摸底排查工作的通知为深入贯彻落实关于各地开展干部职工思想状况大摸底大排查情况上的批示要求和改革教育第二次调度会议精神,有针对性做好队伍教育管...
【三个代表】 日期:2024-03-18
-
 2024年公路养护中心主任典型事迹材料(完整文档)
2024年公路养护中心主任典型事迹材料(完整文档)
“中心的工作就是心中的事业”——公路养护中心主任典型事迹材料**,男,1976年6月出生,1993年参加工作,2000年4月调入**区交通运输局工作,大学本科学历,中共党员,现任**...
【马克思主义】 日期:2024-03-17
